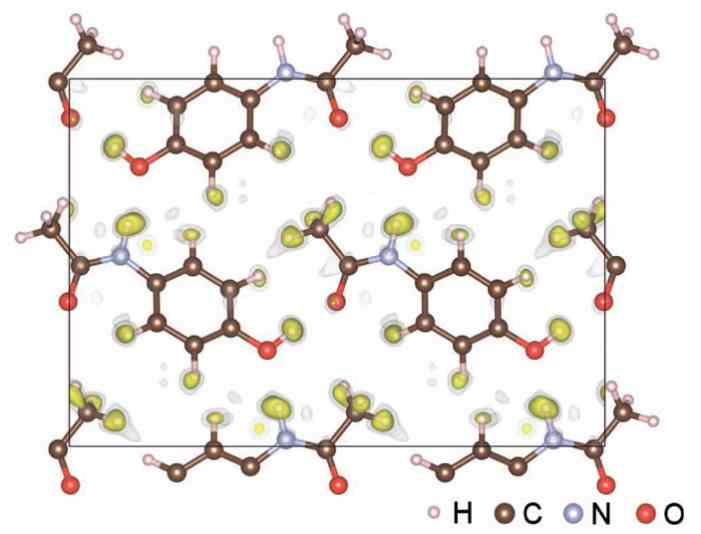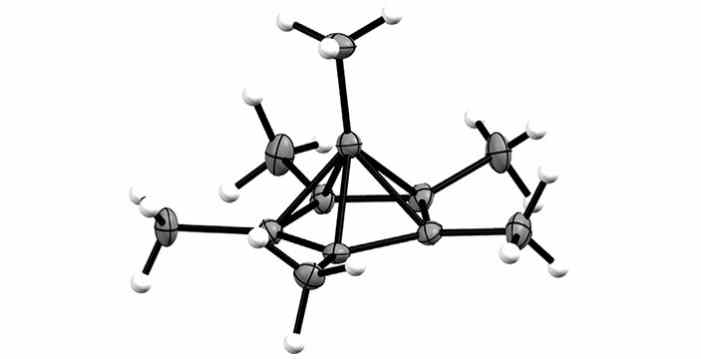
Рис. 1. Структура гексаметил-бензольного дикатиона с шестикоординационным углеродом полученная рентгенокристаллографией. Стальные эллипсоиды — атомы углерода, белые шары — атомы водорода. Схема из обсуждаемой статьи в Angewandte Chemie
Исследователи из Берлинского университета синтезировали и ввели структуру гексаметил-бензольного дикатиона. Это — бензол без двух электронов, к какому вместо атомов водорода прикреплены шесть метильных групп СН3. Такая структура является исключением разом из двух важных правил органической химии: (1) в ней не четырехкоординационный углерод, а шестикоординационный; (2) это не плоское, не шестиугольное производное бензола (эта особенность уникальна).
Фридрих Август Кекуле — одинешенек из наиболее известных химиков в истории, автор теории валентности. Собственно он установил, в частности, что атом углерода четырехвалентен, то есть способен основывать не более четырех связей. Это правило живо по сей день, и автору собственно не раз приходилось снижать оценку студентам, рисовавшим углерод с пятью и шестью связями. Но вернемся к Кекуле. Вяще всего его имя ассоциируется со структурой молекулы бензола — плоской шестиугольной молекулы из шести атомов углерода и шести атомов водорода (рис. 2, A). Кекуле установил ее структуру в 1865 году, не имея почти никаких приборов, и эта труд вдохновляет химиков по сей день. По словам самого Кекуле, на дума о циклическом строении бензола его навело видение уробороса. Правило «плоскости» и «шестиугольности» бензольного перстни вошло в органическую химию так же, как и правило четырехвалентности углерода. Таковы все популярные производные бензола.
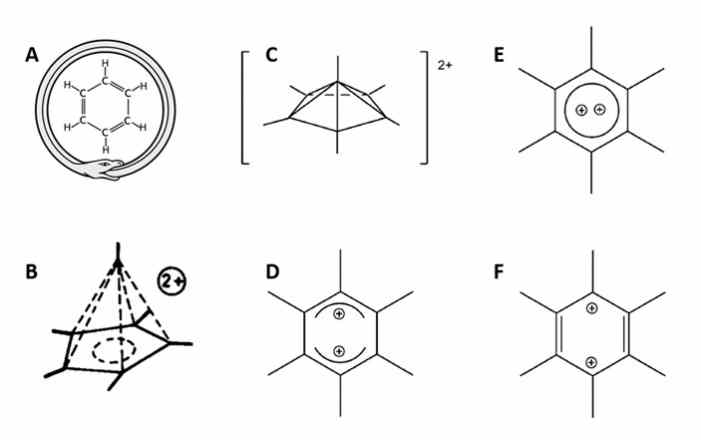
Рис. 2. А — бензол с обвившимся вокруг него уроборосoм, рисунок с сайта en.wikipedia.org. В — структура гексаметил-бензольного дикатиона, предложенная голландской группой в 1973 году, рисунок из статьи H. Hogeveen, P. W. Kwant, 1973. Direct observation of a remarkably stable dication of unusual structure: (CCH3)62+. С — схематическое изображение структуры с рис. 1; в углах и на крышках линий располагаются атомы углерода, атомы водорода не показаны. D, Е, F — альтернативные (не замеченные) варианты строения дикатиона бензола. Квантомеханические расчеты показали, что такие структуры еще немного стабильны, чем полученная. Схемы из обсуждаемой статьи в Angewandte Chemie
Однако, наука она на то и наука, чтобы опровергать правила или желая бы искать из них исключения. Cо времен Кекуле исключений из правила четырехвалентности углерода было отыскано немало (хотя и не сказать, чтоб уж очень много). Даже в натуре как минимум одно такое исключение существует (см. Расшифрована структура каталитического середины нитрогеназы — фермента, расщепляющего атмосферный азот, «Элементы», 22.11.2011).
Но правило плоского шестиугольного бензола очутилось куда «крепче». Первый намек на возможное исключение из него показался в 1973 году, когда голландская группа химиков заявила о получении гексаметил-бензольного дикатиона, и эти спектроскопии этого вещества не подходили под плоскую шестиугольную модель. Авторы предположили неклассичиское пирамидальное постройка с шестикоординационным углеродом (рис. 2, B), но молекула была крайне нестабильна и молекулярную структуру тогда дешифровать не смогли. А без расшифрованной молекулярной структуры в химии доказать гипотезу весьма тяжело — слишком много может быть неучтенных вариантов.
Лишь недавно, в конце 2016 года, группе из Берлинского университета удалось то, что не удалось голландцам в 1973-м. Несколько изменив обстоятельства синтеза, они выделили монокристаллы интригующей молекулы при −78°С и исследовали их при подобный же низкой температуре, чтобы избежать распада. Расшифрованная структура целиком подтвердила предположение голландцев и, наверное, расстроила уверенных в непогрешимости правила Кекуле (рис. 1, рис. 2, C). Квантовомеханические расчеты, проделанные исследователями, показали, что альтернативные классические плоские шестиугольные структуры дикатиона (рис. 2, D, Е, F) намного (от 80 до 130 kJ/mol) немного стабильны, чем полученная структура.
Такой нестабильной молекуле, разумеется, никакого применения не светит. Но полученные знания очень могут сгодиться для определения родственных структур и для понимания механизмов важных реакций бензольных производных, в каких подобные молекулы могут быть промежуточными.